
在一定体积的密闭容器中,进行如下化学反应: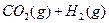

 ,其化学平衡常数K和温度T的关系如下表:
,其化学平衡常数K和温度T的关系如下表:
T/℃
700
800
830
1000
1200
K
0.6
0.9
1.0
1.7
2.6 回答下列问题:
(1)该反应的化学平衡常数表达式为K= 。(2)该反应为 (填“吸热”或“放热”)反应。(3)能判断该反应已达到化学平衡状态的依据是( )
A.容器中压强不变
B.混合气体中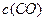 不变
不变
C.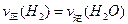
D.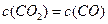 (4)某温度下,平衡浓度符合下式:
(4)某温度下,平衡浓度符合下式:
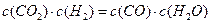 ,试判断此时的温度为 ℃。
,试判断此时的温度为 ℃。
相关专题: 化学平衡


相关问题推荐
已知N2(g)+3H2(g) 2NH3(g),现向一密闭容器中充入1molN2和3molH2,在高温、高压和催化剂存在条件下发生反应。下列有关说法正确的是
2NH3(g),现向一密闭容器中充入1molN2和3molH2,在高温、高压和催化剂存在条件下发生反应。下列有关说法正确的是
A.最终可以生成2molNH3
B.达到化学平衡状态时,正反应和逆反应的速率都为0
C.达到化学平衡状态时,容器中N2、H2和NH3的物质的量之比为1∶3∶2
D.达到化学平衡状态时,N2、H2和NH3的物质的量浓度不再变化
一定温度下,在容积不变的密闭容器中充入lmolN2和3molH2,发生合成氨反应,t分钟后达到平衡状态。下列有关说法正确的是
A.达到化学平衡状态时,容器中将生成2molNH3
B.t分钟后,只要条件不变,容器内各气体的浓度就不再变化
C.达到化学平衡状态时,v(N2)=v(H2)=v(NH3)
D.达到化学平衡状态时,正反应和逆反应的速率相等,且均等于0
下列哪种表述化学平衡常数的特性是错误的()
A、化学平衡常数与反应物的最初浓度无关
B、化学平衡常数与平衡状态时生成物的最初浓度无关
C、温度可改变化学平衡常数
D、对于有固体物质参加的多相可逆反应,化学上规定纯固体的浓度等于1
可逆反应mA(s)+nB(g) cC(g)+fD(g)反应过程中,当其它条件不变时,C的体积分数(C%)与温度(T)和压强_(_P_)_的关系如下图所示(T2>T1),下列叙述错误的是( )
cC(g)+fD(g)反应过程中,当其它条件不变时,C的体积分数(C%)与温度(T)和压强_(_P_)_的关系如下图所示(T2>T1),下列叙述错误的是( )
A.达到平衡后,若使用催化剂,C的体积分数增大
B.达到平衡后,若使温度升高,化学平衡向逆反应方向移动
C.化学方程式中n<c+f
D.达到化学平衡后,增加A的量有利于化学平衡向正反应方向移动
(4分)在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)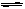 CO(g)+H2O(g)其化学平衡常数K与温度t的关系如下表:
CO(g)+H2O(g)其化学平衡常数K与温度t的关系如下表:
t/℃
700
800
830
1000
1200
K
0.6
0.9
1.0
1.7
2.6回答下列问题:
(1)该反应的化学平衡常数表达式为K= 。(2)该反应为 反应(填“吸热”“放热”)。



