
问题详情
一定条件下,在2SO2(g) + O2(g)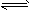 2SO3(g) 的化学平衡体系中,各物质的浓度分别为: C(SO2)=2.0 mol/L,C(O2)= 0.8 mol/L,C(SO3)= 2.4mol/L,则氧气的起始时的浓度可能是
2SO3(g) 的化学平衡体系中,各物质的浓度分别为: C(SO2)=2.0 mol/L,C(O2)= 0.8 mol/L,C(SO3)= 2.4mol/L,则氧气的起始时的浓度可能是
[ ]
A.0.8-2.4 mol/L B.0-2 mol/L C.0-0.8 mol/L D.无法确定
相关专题: 化学平衡
未搜索到的试题可在搜索页快速提交,您可在会员中心"提交的题"快速查看答案。
收藏该题
查看答案

搜题

相关问题推荐
对于反应2SO2+O2 2SO3,判断下列说法正确的是( )①单位时间内生成2molSO2,同时生成1molO2,则处于化学平衡状态 ②SO2生成速率等于SO2消耗速率,则处于化学平衡状态 ③SO2、O2、SO3的体积分数不再发生变化,则处于化学平衡状态 ④SO2、O2、SO3的分子数之比为2∶1∶2,则处于化学平衡状态
2SO3,判断下列说法正确的是( )①单位时间内生成2molSO2,同时生成1molO2,则处于化学平衡状态 ②SO2生成速率等于SO2消耗速率,则处于化学平衡状态 ③SO2、O2、SO3的体积分数不再发生变化,则处于化学平衡状态 ④SO2、O2、SO3的分子数之比为2∶1∶2,则处于化学平衡状态
A.①③
B.②④
C.②③
D.③④
在一定体积的密闭容器中,进行如下化学反应: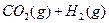

 ,其化学平衡常数K和温度T的关系如下表:
,其化学平衡常数K和温度T的关系如下表:
T/℃
700
800
830
1000
1200
K
0.6
0.9
1.0
1.7
2.6 回答下列问题:
(1)该反应的化学平衡常数表达式为K= 。(2)该反应为 (填“吸热”或“放热”)反应。(3)能判断该反应已达到化学平衡状态的依据是( )
A.容器中压强不变
B.混合气体中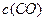 不变
不变
C.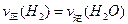
D.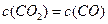 (4)某温度下,平衡浓度符合下式:
(4)某温度下,平衡浓度符合下式:
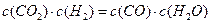 ,试判断此时的温度为 ℃。
,试判断此时的温度为 ℃。
关于化学平衡状态和化学反应限度的说法正确的是
A.当一个可逆反应达到化学平衡状态时,正向反应速率和逆向反应速率都等于零
B.一个可逆反应达到的平衡状态就是这个反应在该条件下所能达到的限度
C.化学平衡状态时,各物质的浓度保持相等
D.化学反应的限度由反应物的本性决定,是不可改变的



