
已知:①1molH2分子中化学键断裂时需要吸收436kJ的能量 ②1molCl2分子中化学键断裂时需要吸收243kJ的能量 ③由H原子和Cl原子形成1molHCl分子时释放431kJ的能量。 下列叙述正确的是()。
A、氢气和氯气反应生成氯化氢气体的热化学方程式是H2(g)+Cl2(g)2HCl(g)
B、氢气和氯气反应生成2mol氯化氢气体,反应的ΔH=+183kJ·mol-l
C、氢气和氯气反应生成2mol氯化氢气体,反应的ΔH=-183kJ·mol-l
D、氢气和氯气反应生成1mol氯化氢气体,反应的AH=+183kJ·mol-l
相关专题: 氯化氢 化学键


相关问题推荐
石油化工是江苏省的支柱产业之一。聚氯乙烯是用途十分广泛的石油化工产品,某化工厂曾利用下列工艺生产聚氯乙烯的单体氯乙烯:
CH2=CH2+Cl2→CH2Cl-CH2Cl…………………①
CH2Cl-CH2Cl→CH2=CHCl+HCl………………②
请回答以下问题:
(1)已知反应①中二氯乙烷的产率(产率=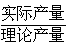 ×100%)为98%,反应②中氯乙烯和氯化氢的产率均为95%,则2.8t乙烯可制得氯乙烯____\__t,同时得到副产物氯化氢______t。(计算结果保留1位小数)
×100%)为98%,反应②中氯乙烯和氯化氢的产率均为95%,则2.8t乙烯可制得氯乙烯____\__t,同时得到副产物氯化氢______t。(计算结果保留1位小数)
(2)为充分利用副产物氯化氢,该工厂后来将下列反应运用于生产:
2CH2=CH2+4HCl+O2→2CH2Cl-CH2Cl+2H2O………③
由反应①、③获得二氯乙烷,再将二氯乙烷通过反应②得到氯乙烯和副产物氯化氢,副产物氯化氢供反应③使用,形成了新的工艺。由于副反应的存在,生产中投入的乙烯全部被消耗时,反应①、③中二氯乙烷的产率依次为a%、c%;二氯乙烷全部被消耗时,反应②中氯化氢的产率为b%。试计算:反应①、③中乙烯的投料比为多少时,新工艺既不需要购进氯化氢为原料,又没有副产物氯化氢剩余(假设在发生的副反应中既不生成氯化氢,也不消耗氯化氢)。
在1升氯化氢水溶液中,已知溶解了氯化氢气体268.4升(标准状况),所得溶液的密度为1.19克/厘米3,此溶液中氯化氢的质量分数为____,物质的量浓度为____.
下列哪些物质是氯化副产物()
A、氯仿、酸性氯化呋喃
B、卤化氢、氯化氢
C、酸性氯化呋喃、环己烷
D、卤化氢、氯化钾
E、二氯化氢、溴仿
背景材料: 以下是李老师的《化学能与热能》的教学片段: [创设问题情景] 氢气和氯气的混合气体遇到强光会发生什么现象?为什么? [学生思考、讨论] 氢气和氯气的混合气体遇到强光会发生爆炸。这是因为反应在有限的空间里进行,放出大量的热,使周围气体急剧膨胀。 [进一步思考] 反应中的热量由何而来?氢气和氯气反应的本质是什么? [学生思考、讨论] 从化学键角度分析氢气和氯气反应的本质。 板书:一、化学键与化学反应中能量的变化关系 [教师补充讲解] 化学反应的本质是反应物中化学键的断裂和生成物中化学键的形成。化学键是物质内部微粒之间强烈的相互作用,断开反应物中的化学键需要吸收能量,形成生成物中的化学键要放出能量。氢气和氯气反应的本质是在一定的条件下,氢气分子和氯气分子中的H-H键和Cl-Cl键断开,氢原子和氯原子通过形成H-Cl键而结合成HCl分子。1molH2中含有1molH-H键,1molCl2中含有1molCl-Cl键,在25℃和101kPa的条件下,断开1molH-H键要吸收436kJ的能量,断开1molCl-Cl键要吸收242kJ的能量,而形成1molHCl分子中的H-Cl键会放出431kJ的能量。这样,由于破坏旧键吸收的能量少于形成新键放出的能量,根据“能量守恒定律”,多余的能量就会以热量的形式释放出来。 [归纳小结] 1.化学键的断裂和形成是化学反应中能量变化的主要原因。 2.能量是守恒的。 [练习反馈] 已知断开lmolH2中的化学键要吸收436kJ的能量,断开1molO2中的化学键要吸收496kJ的能量,形成水分子中的1molH-O键要放出463kJ的能量,试说明中的能量变化。 [讲解] 刚才我们从微观的角度分析了化学反应中能量变化的主要原因,那么,又怎样从宏观的角度来判断一个反应到底是放热还是吸热的呢?各种物质中都含有化学键,因而我们可以理解为各种物质中都储存有化学能。化学能是能量的一种形式,它可以转化为其他形式的能量。不同物质由于组成、结构不同,因而所包含的化学能也不同。在化学反应中,随着物质的变化,化学能也随之改变,如H2与Cl2、O2的反应。那么,一个化学反应吸收能量还是放出能量是由什么决定的呢? [学生讨论、交流] 1.一个确定的化学反应在发生过程中是吸收能量还是放出能量取决于反应物的总能量和生成物的总能量的相对大小。 2.画出反应物、生成物总能量的大小与反应中能量变化的关系示意图。 [思考与分析] 甲烷燃烧要放出热量,水电解产生氢气和氧气,试从化学键和物质所含能量的角度分析其原因,并说明反应过程中能量的转变形式。 [提出问题] 前面我们通过对具体反应的分析,从微观和宏观两个角度探讨了化学反应中能量变化的主要原因,知道了化学能和其他能量是可以相互转变的,还知道化学反应中能量变化通常表现为热量的变化。那么,怎样把物质变化和热量变化统一地表达出来呢?你可以在和同学讨论的基础上提出自己的想法,并对其他同学提出的表达方式做出评价。 问题: (1)写出通过本课的学习,学生可以获得怎样的知识与技能。 (2)说明本课的教学重点和难点。 (3)李老师所采用的教学方法有哪些? (4)请列举出常见的吸热反应和放热反应。
垃圾焚烧厂余热锅炉出口烟气量为67000m3(标况)/h,其中含二氧化硫85mg/m3,氯化氢150mg/m3,经过脱酸反应后,二氧化硫去除率为80%,氯化氢去除率为95%,计算净化后烟气二氧化硫、氯化氢的含量各为多少mg/m3。()
A、68.0,142.5
B、17.0,7.5
C、142.5,68.0
D、7.5,17.0



